Ticarət adı: Semavic®
Beynəlxalq patentləşdirilməmiş adı (BPA): semaqlutid
Dərman forması: dərialtı yeridilmə üçün məhlul
Tərkibi: 1 ml məhlulda aşağıdakı maddələr vardır: təsiredici maddə: semaqlutid – 1,34 mq; köməkçi maddələr: dinatrium hidrofosfat dihidrat – 1,42 mq, propilenqlikol – 14,0 mq, fenol – 5,5 mq, durulaşdırılmış 10 %-li xlorid turşusu və/və ya 10 %-li natrium hidroksid məhlulu (pH-ın 7,4-dək tənzimlənməsi üçün), inyeksiya üçün su – 1 ml-dək.
Təsviri: Şəffaf, rəngsiz və ya demək olar ki, rəngsiz məhlul.
Dərman preparatının farmakoterapevtik qrupu: Hipoqlikemik vasitə – qlükaqonabənzər peptid -1-in (QBP-1) analoqu.
ATK kodu: А10В106.
Farmakoloji xüsusiyyətləri
Semaqlutid QBP-1 reseptorlarının (QBP-1R) kimyəvi sintez yolu ilə istehsal edilmiş aqonistidir. Semaqlutid insan QBP-1-i ilə 94 % homolojiliyə malik olan QBP-1 analoqudur. Semaqlutid QBP-1R ilə seçici olaraq birləşən və onu aktivləşdirən QBP-1R aqonisti kimi təsir edir. QBP-1R təbii QBP-1 üçün hədəf rolunu oynayır. QBP-1 qlükozanın konsentrasiyasının və iştahanın tənzimlənməsinə, eləcə də ürək-damar sisteminə (ÜDS) eyni zamanda bir neçə cür təsir göstərən fizioloji hormondur. Qlükozanın konsentrasiyasına və iştahaya təsir spesifik olaraq mədəaltı vəzidə və beyində yerləşən QBP-1R vasitəsilə həyata keçirilir. Semaqlutidin farmakoloji konsentrasiyaları aşağıda təsvir edilmiş təsirlərin birləşməsi vasitəsilə qanda qlükozanın konsentrasiyasını və bədən çəkisini aşağı salır. QBP-1R həmçinin ürəyin, damarların, immun sisteminin və böyrəklərin xüsusi nahiyələrində yerləşmişdir ki, burada onların aktivləşməsi ürək-damar (ÜD) sisteminə və mikrosirkulyasiyaya təsirlərə səbəb ola bilər. Təbii QBP-1-dən fərqli olaraq, semaqlutidin uzadılmış yarımxaricolma müddəti (1 həftəyə yaxın) onu həftədə 1 dəfə dərialtı (d/a) inyeksiya şəklində yeritməyə imkan verir. Albuminlə birləşmə semaqlutidin uzunmüddətli təsirinin əsas mexanizmidir ki, bu da onun böyrəklər tərəfindən xaric edilməsinin azalmasına gətirib çıxarır və metabolik parçalanmadan qoruyur. Bundan əlavə, semaqlutid dipeptidilpeptidaza-4 fermenti tərəfindən parçalanma baxımından sabitdir. Semaqlutid qanda qlükozanın konsentrasiyasını insulin sekresiyasının qlükozadan asılı stimullaşdırılması və qlükaqon sekresiyasının qlükozadan asılı inhibə olunması vasitəsilə aşağı salır. Beləliklə, qanda qlükozanın konsentrasiyası artdıqda insulin sekresiyasının stimullaşdırılması və qlükaqon sekresiyasının inhibə olunması baş verir. Qlikemiyanın səviyyəsinin azaldılması mexanizminə həm də erkən postprandial fazada mədə boşalmasının bir qədər ləngiməsi də daxildir. Hipoqlikemiya zamanı semaqlutid insulinin sekresiyasını azaldır və qlükaqonun sekresiyasını azaltmır. Semaqlutid enerji sərfini azaltmaqla ümumi bədən çəkisini və piy toxumasının kütləsini azaldır. Bu mexanizm iştahanın ümumi azalmasını, o cümlədən doyma siqnallarının güclənməsini və aclıq siqnallarının zəifləməsini, eləcə də qida qəbuluna nəzarətin yaxşılaşmasını və qidaya qarşı meylin azalmasını ehtiva edir. Bununla yanaşı, çox güman ki, bədən çəkisinin azalması sayəsində, insulinə qarşı rezistentlik də azalır. Bundan əlavə, semaqlutid tərkibində yağların miqdarı yüksək olan qidaların qəbuluna üstünlük verilməsini azaldır. Heyvanlar üzərində aparılmış tədqiqatlarda göstərilmişdir ki, semaqlutid baş beyinin xüsusi nahiyələri tərəfindən udulur, əsas toxluq siqnallarını gücləndirir və əsas aclıq siqnallarını zəiflədir. Semaqlutid baş beyin toxumalarının ayrı-ayrı sahələrinə təsir edərək, toxluq hissi ilə əlaqəli neyronları aktivləşdirir və aclıq hissi ilə əlaqəli neyronları inhibə edir. Klinik tədqiqatlarda (KT) semaqlutid qan plazmasının lipidlərinə müsbət təsir göstərmiş, sistolik arterial təzyiqi (AT) aşağı salmış və iltihabı azaltmışdır. Heyvanlar üzərində aparılan tədqiqatlarda semaqlutid aorta piləklərinin sonrakı inkişafının qarşısını almaq və piləklərdə iltihabı azaltmaqla aterosklerozun inkişafını zəiflədir.
Farmakodinamika
Bütün farmakodinamik tədqiqatlar 12 həftəlik müalicədən sonra (dozanın artırılması dövrü də daxil olmaqla), semaqlutidin 1 mq dozada həftədə 1 dəfə yeridilməsi ilə tarazlıq konsentrasiyasında aparılmışdır.
Acqarına vəziyyətdə qlikemiyanın səviyyəsi və postprandial qlikemiyanın səviyyəsi
Semaqlutid acqarına vəziyyətdə qlükozanın konsentrasiyasını və qlükozanın postprandial konsentrasiyasını azaldır. Tip 2 şəkərli diabeti (ŞD2) olan pasiyentlərdə plasebo ilə müqayisədə 1 mq semaqlutid ilə müalicə ilkin dəyərə nisbətən mütləq dəyişiklik baxımından qlükozanın konsentrasiyasının azalmasına (mmol/l) və aşağıdakılar baxımından plasebo ilə müqayisədə nisbi azalmaya (%) gətirib çıxarmışdır: acqarına vəziyyətdə qlükozanın konsentrasiyası (1,6 mmol/l; 22 %); qida qəbulundan 2 saat sonra qlükozanın konsentrasiyası (4,1 mmol/l; 37 %); qlükozanın orta gündəlik konsentrasiyası (1,7 mmol/l; 22 %) və 3 qida qəbulu ərzində qlükozanın konsentrasiyasının postprandial pik səviyyələri (0,6–1,1 mmol/l). Semaqlutid birinci dozanın yeridilməsindən sonra acqarına vəziyyətdə qlükozanın konsentrasiyasını azaltmışdır.
Mədəaltı vəzinin beta-hüceyrələrinin funksiyası və insulinin sekresiyası
Semaqlutid acqarına vəziyyətdə qlükozanın konsentrasiyasını və qlükozanın postprandial konsentrasiyasını azaldır. Tip 2 şəkərli diabeti (ŞD2) olan pasiyentlərdə plasebo ilə müqayisədə 1 mq semaqlutid ilə müalicə ilkin dəyərə nisbətən mütləq dəyişiklik baxımından qlükozanın konsentrasiyasının azalmasına (mmol/l) və aşağıdakılar baxımından plasebo ilə müqayisədə nisbi azalmaya (%) gətirib çıxarmışdır: acqarına vəziyyətdə qlükozanın konsentrasiyası (1,6 mmol/l; 22 %); qida qəbulundan 2 saat sonra qlükozanın konsentrasiyası (4,1 mmol/l; 37 %); qlükozanın orta gündəlik konsentrasiyası (1,7 mmol/l; 22 %) və 3 qida qəbulu ərzində qlükozanın konsentrasiyasının postprandial pik səviyyələri (0,6–1,1 mmol/l). Semaqlutid birinci dozanın yeridilməsindən sonra acqarına vəziyyətdə qlükozanın konsentrasiyasını azaltmışdır.
Qlükaqonun sekresiyası
Semaqlutid acqarına vəziyyətdə qlükaqonun konsentrasiyasını və qlükaqonun postprandial konsentrasiyasını azaldır. ŞD2 olan pasiyentlərdə semaqlutid qlükaqonun konsentrasiyasının plasebo ilə müqayisədə nisbi azalmasına gətirib çıxarır: acqarına vəziyyətdə qlükaqonun konsentrasiyası (8–21 %), postprandial qlükaqon cavabı (14–15 %) və qlükaqonun orta gündəlik konsentrasiyası (12 %).
İnsulinin qlükozadan asılı sekresiyası və qlükaqonun qlükozadan asılı sekresiyası
Semaqlutid insulinin sekresiyasını qlükozadan asılı üsulla stimullaşdırmaq və qlükaqonun sekresiyasını qlükozadan asılı üsulla azaltmaq yolu ilə qanda qlükozanın yüksək konsentrasiyasını aşağı salmışdır. ŞD2 olan pasiyentlərə semaqlutidin yeridilməsindən sonra insulin sekresiyasının sürəti sağlam könüllülərdəki ilə oxşar olmuşdur. İnduksiya edilmiş hipoqlikemiya zamanı semaqlutid plasebo ilə müqayisədə qlükaqonun konsentrasiyasının artmasının əks-tənzimləyici cavabını dəyişdirməmiş, eləcə də ŞD2-li pasiyentlərdə C-peptidin konsentrasiyasının azalmasını gücləndirməmişdir.
Mədənin boşalması
Semaqlutid erkən postprandial dövrdə mədə boşalmasının bir qədər ləngiməsinə səbəb olmuş və bununla da postprandial qlükozanın qana daxil olma sürətini azaltmışdır.
Bədən çəkisi və bədən tərkibi
Tədqiq edilmiş müqayisə preparatları (plasebo, sitaqliptin, ləng azad olan (LA) eksenatid, dulaqlutid və insulin qlarqin) ilə müqayisədə semaqlutidin istifadəsi zamanı bədən çəkisinin daha çox azalması müşahidə olunmuşdur (“Klinik effektivlik və təhlükəsizlik” bölməsinə baxın). Semaqlutidin istifadəsi zamanı bədən çəkisinin azalması başlıca olaraq, əzələ toxumasının itirilməsindən 3 dəfə artıq olan piy toxumasının itirilməsi sayəsində baş vermişdir.
İştaha, kalori istehlakı və ərzaq məhsullarının seçilməsi
Plasebo ilə müqayisədə semaqlutid üç ardıcıl ad libitum qida qəbulu ərzində kalori istehlakını 18–35 % azaltmışdır. Buna semaqlutidin həm acqarına vəziyyətdə, həm də qida qəbulundan sonra iştahanın azalmasına stimullaşdırıcı təsiri, qida qəbuluna nəzarətin yaxşılaşması, yeməyə, xüsusilə də, tərkibində yağların miqdarı yüksək olan yeməklərə qarşı meylin azalması səbəb olmuşdur.
Acqarına vəziyyətdə lipidlər və postprandial lipidlər
Plasebo ilə müqayisədə semaqlutid acqarına vəziyyətdə triqliseridlərin və çox aşağı sıxlıqlı lipoproteinlərin (ÇASLP) xolesterininin konsentrasiyasını müvafiq olaraq 12 % və 21 % azaltmışdır. Tərkibində yağların miqdarı yüksək olan qida qəbuluna cavab olaraq triqliseridlərin və çox aşağı sıxlıqlı lipoproteinlərin (ÇASLP) xolesterininin konsentrasiyasının postprandial artması 40 %-dən çox azalmışdır.
Ürəyin elektrofiziologiyası (ÜEF)
Semaqlutidin ürəkdə repolyarizasiya prosesinə təsiri ÜEF müayinəsində sınaqdan keçirilmişdir. Semaqlutidin terapevtik dozalardan yüksək olan dozalarda istifadəsi (1,5 mq-a qədər tarazlıq konsentrasiyasında) korreksiya olunmuş QT intervalının uzanmasına gətirib çıxarmamışdır.
Farmakokinetika
Preparat həftədə 1 dəfə yeridilmək üçün uyğundur, belə ki, semaqlutidin yarımxaricolma müddəti təxminən 1 həftəyə bərabərdir.
Sorulma
Plazmada maksimal konsentrasiyanın (Cmax) əldə olunma müddəti preparatın dozasının yeridilməsindən sonra 1 gündən 3 günədək təşkil etmişdir. Preparatın tarazlıq konsentrasiyası (AUCt/24) preparatın 4–5 həftə ərzində həftədə bir dəfə yeridilməsindən sonra əldə edilmişdir. Semaqlutidin 0,5 mq və 1 mq dozalarda d/a yeridilməsindən sonra ŞD2 olan pasiyentlərdə onun tarazlıq konsentrasiyasının orta göstəriciləri müvafiq olaraq 16 nmol/l və 30 nmol/l təşkil etmişdir. Semaqlutidin 0,5 mq və 1 mq dozaları üçün ekspozisiya yeridilmiş dozaya mütənasib olaraq artır. Semaqlutidin qarının ön divarına, buda və ya bazuya d/a yeridilməsi zamanı oxşar ekspozisiya əldə edilir. D/a yeridilmədən sonra semaqlutidin mütləq biomənimsənilməsi 89 % təşkil etmişdir.
Paylanma
ŞD2 olan pasiyentlərə d/a yeridildikdən sonra semaqlutidin toxumalarda orta paylanma həcmi təxminən 12,5 l təşkil etmişdir. Semaqlutid qan plazmasının albumini ilə əhəmiyyətli dərəcədə (>99 %) birləşmişdir.
Biotransformasiya
Semaqlutid zülalın peptik əsasının proteolitik parçalanması və daha sonra yan zəncirin yağ turşusunun beta-oksidləşməsi vasitəsilə metabolizə olunur.
Xaric olması
Mədə-bağırsaq traktı (MBT) və böyrəklər semaqlutidin və onun metabolitlərinin orqanizmdən çıxarılmasının əsas yollarıdır. Semaqlutidin yeridilmiş dozasının 2/3 hissəsi böyrəklər və 1/3 hissəsi bağırsaq vasitəsilə xaric olunur. Yeridilmiş dozanın təxminən 3 %-i dəyişilməmiş semaqlutid şəklində böyrəklər tərəfindən xaric edilir. ŞD2 olan pasiyentlərdə semaqlutidin klirensi təxminən 0,05 l/saat təşkil etmişdir. Təxminən 1 həftəlik eliminasiya yarımxaricolma müddəti ilə semaqlutid preparatın sonuncu dozasının yeridilməsindən sonra təxminən 5 həftə ərzində ümumi qan dövranında mövcud olacaqdır.
Pasiyentlərin xüsusi qrupları
Pasiyentin yaşından, cinsindən, irqi və etnik mənsubiyyətindən, bədən çəkisindən, böyrək və ya qaraciyər çatışmazlığının olub-olmamasından asılı olmayaraq semaqlutidin dozasının tənzimlənməsi tələb olunmur.
Yaş
20 yaşdan 86 yaşadək pasiyentlərin iştirakı ilə keçirilmiş 3a fazası KT-nin gedişində əldə edilmiş məlumatlara əsasən, pasiyentin yaşı semaqlutidin farmakokinetikasına təsir etməmişdir.
Cins
Pasiyentin cinsi semaqlutidin farmakokinetikasına təsir etməmişdir.
İrq
İrq qrupu (ağdərili, qaradərili və ya afroamerikalı, asiyalı) semaqlutidin farmakokinetikasına təsir etməmişdir.
Etnik mənsubiyyət
Etnik mənsubiyyət (latınamerikalı) semaqlutidin farmakokinetikasına təsir etməmişdir.
Bədən çəkisi
Bədən çəkisi semaqlutidin farmakokinetikasına təsir etməmişdir. Daha yüksək bədən çəkisi daha aşağı ekspozisiyaya gətirib çıxarır. Semaqlutidin 0,5 mq və 1 mq dozaları bədən çəkisinin 40–198 kq diapazonunda preparatın yetərli ekspozisiyasını təmin edir.
Böyrək çatışmazlığı
Böyrək çatışmazlığı semaqlutidin farmakokinetikasına klinik cəhətdən əhəmiyyətli təsir göstərməmişdir. Bu, semaqlutidin 0,5 mq birdəfəlik dozası ilə aparılmış tədqiqatda böyrək funksiyası normal olan pasiyentlərlə müqayisədə müxtəlif dərəcəli böyrək çatışmazlığı olan pasiyentlərdə (yüngül, orta, ağır və ya dializdə olan pasiyentlərdə) göstərilmişdir. Bu, həmçinin 3a fazası KT-nin məlumatlarına əsasən, ŞD2 və böyrək çatışmazlığı olan pasiyentlər üçün göstərilmişdir, halbuki böyrək xəstəliyinin son mərhələsində olan pasiyentlərdə istifadə təcrübəsi məhdud olmuşdur.
Qaraciyər çatışmazlığı
Qaraciyər çatışmazlığı semaqlutidin farmakokinetikasına təsir etməmişdir. Semaqlutidin farmakokinetik xüsusiyyətləri semaqlutidin 0,5 mq birdəfəlik dozası ilə aparılmış tədqiqatlarda qaraciyər funksiyası normal olan pasiyentlərlə müqayisədə müxtəlif dərəcəli qaraciyər çatışmazlığı olan pasiyentlərdə (yüngül, orta, ağır) qiymətləndirilmişdir.
Uşaqlar və yeniyetmələr
18 yaşadək uşaq və yeniyetmələrdə semaqlutidin tədqiqatları aparılmamışdır.
İstifadəsinə göstərişlər
Semavic® preparatı tip 2 şəkərli diabeti olan böyüklərdə qlikemik nəzarətin yaxşılaşdırılması üçün pəhriz və fiziki hərəkətlər fonunda aşağıdakı formalarda istifadə üçün göstərişdir:
Semavic® preparatı tip 2 şəkərli diabetlə yanaşı ürək-damar xəstəliklərinin riski yüksək olan pasiyentlərdə ürək-damar xəstəliklərinin standart müalicəsinə əlavə qismində böyük ürək-damar hadisələrinin* inkişaf etməsi riskinin azaldılması üçün göstərişdir (birinci böyük ürək-damar hadisəsinin baş vermə vaxtının təhlilinə əsasən – “Farmakoloji xüsusiyyətlər” bölməsinə, “ÜDS-yə təsirin qiymətləndirilməsi” alt bölməsinə baxın).
*böyük ürək-damar hadisələrinə aşağıdakılar daxildir: ürək-damar patologiyası səbəbindən ölüm, ölümlə nəticələnməyən miokard infarktı, ölümlə nəticələnməyən insult.
Əks-göstərişlər
Effektivlik və təhlükəsizlik üzrə məlumatların olmaması və ya məhdud istifadə təcrübəsi səbəbindən aşağıdakı pasiyent qruplarında və aşağıdakı vəziyyətlər/ xəstəliklər zamanı Semavic® preparatının istifadəsi əks-göstərişdir:
Ehtiyatla
Böyrək çatışmazlığı olan pasiyentlərdə və anamnezində pankreatit olan pasiyentlərdə Semavic® preparatını ehtiyatla istifadə etmək tövsiyə olunur (“Xüsusi göstərişlər” bölməsinə baxın).
Hamiləlik və laktasiya dövrlərində istifadəsi
Hamiləlik
Heyvanlar üzərində aparılmış tədqiqatlar preparatın reproduktiv toksikliyə malik olduğunu nümayiş etdirmişdir (“Təhlükəsizlik üzrə preklinik məlumatlar” bölməsinə baxın). Hamilə qadınlarda semaqlutidin istifadəsinə dair məlumatlar məhdud həcmdədir. Hamiləlik dövründə semaqlutidin istifadəsi əks-göstərişdir. Reproduktiv potensialı saxlanılmış qadınların semaqlutid ilə müalicə müddətində kontrasepsiya vasitələrindən istifadə etmələri tövsiyə olunur. Əgər pasiyent hamiləliyə hazırlaşırsa və ya hamiləlik artıq baş vermişdirsə, semaqlutid ilə müalicə dayandırılmalıdır. Yarımxaricolma müddətinin uzun olması səbəbindən semaqlutid ilə müalicə hamiləliyin planlaşdırılan başlanmasından ən azı 2 ay əvvəl dayandırılmalıdır (“Farmakokinetika” bölməsinə baxın).
Laktasiya dövrü
Laktasiya dövründə olan siçovullarda semaqlutid ana südünə keçmişdir. Ana südü ilə qidalandırılan uşaq üçün riski istisna etmək olmaz. Laktasiya dövründə semaqlutidin istifadəsi əks-göstərişdir.
İstifadə qaydası və dozaları
İstifadə qaydası
Semavic® preparatı həftədə 1 dəfə, istənilən vaxt, qida qəbulundan asılı olmayaraq istifadə edilir. Semavic® preparatı qarın, bud və ya bazu nahiyələrinə dəri altına (d/a) yeridilir. İnyeksiya yeri dozanın tənzimlənməsi olmadan dəyişdirilə bilər. Semavic® preparatını vena daxilinə və ya əzələ daxilinə yeritmək olmaz. İstifadə qaydası barədə məlumatlar “İstifadə üzrə təlimat” bölməsində göstərilmişdir. Zəruri hallarda, preparatın həftəlik yeridilmə gününü dəyişdirmək olar, bu şərtlə ki, iki inyeksiya arasındakı zaman intervalı ən azı 3 gün (>72 saat) təşkil etsin.
Dozalar
Semavic® preparatının başlanğıc dozası həftədə 1 dəfə 0,25 mq təşkil edir. 4 həftə istifadədən sonra doza həftədə 1 dəfə 0,5 mq-dək artırılmalıdır. Qlikemik nəzarətin sonrakı yaxşılaşdırılması üçün preparatı ən azı 4 həftə ərzində həftədə 1 dəfə 0,5 mq dozada istifadə etdikdən sonra dozanı həftədə 1 dəfə 1 mq-dək artırmaq olar. Semavic® preparatının 0,25 mq dozası terapevtik doza deyildir. Semavic® preparatı monoterapiya şəklində və yaxud bir və ya daha çox hipoqlikemik preparatla kombinasiyada istifadə edilə bilər (“Klinik effektivlik və təhlükəsizlik” bölməsinə baxın). Semavic® preparatı metformin və/və ya tiazolidindionla aparılan əvvəlki müalicəyə əlavə edildikdə, metformin və/və ya tiazolidindionla müalicəni əvvəlki dozalarda davam etdirmək olar. Semavic® preparatı sulfonil sidik cövhəri törəməsi və ya insulinlə aparılan müalicəyə əlavə edildikdə, hipoqlikemiyaların baş vermə riskinin azaldılması məqsədilə sulfonil sidik cövhəri törəməsinin və ya insulinin dozasının azaldılması nəzərə alınmalıdır (“Xüsusi göstərişlər” bölməsinə baxın). Semavic® preparatının istifadəsi qanda qlükozanın konsentrasiyasına pasiyentin özü tərəfindən nəzarət olunmasını tələb etmir. Semavic® preparatının sulfonil sidik cövhəri törəməsi və ya insulinlə kombinasiyada istifadəsi zamanı qanda qlükozanın konsentrasiyasına pasiyentin özü tərəfindən bu cür nəzarət sulfonil sidik cövhəri törəməsinin və ya insulinin dozasının tənzimlənməsi üçün tələb oluna bilər.
Buraxılmış doza
Semavic® preparatının dozası buraxıldığı halda, preparat dozanın planlaşdırılmış yeridilmə anından sonrakı 5 gün ərzində mümkün qədər tez yeridilməlidir. Əgər dozanın buraxılma müddəti 5 gündən çoxdursa, buraxılmış dozanı yeritmək lazım deyil. Semavic® preparatının növbəti dozası adi, planlaşdırılmış gün yeridilməlidir. Hər bir halda pasiyentlər adi, həftədə bir dəfə yeridilmə qrafiklərini bərpa edə bilərlər.
Pasiyentlərin xüsusi klinik qruplarında preparatın istifadəsi
Uşaqlar və yeniyetmələr
Effektivlik və təhlükəsizlik üzrə məlumatların olmaması səbəbindən Semavic® preparatının 18 yaşdan kiçik uşaqlarda istifadəsi əks-göstərişdir.
Yaşlı pasiyentlər (≥65 yaş)
Pasiyentin yaşından asılı olaraq dozanın tənzimlənməsi tələb olunmur. 75 yaş və daha yuxarı pasiyentlərdə semaqlutidin istifadə təcrübəsi məhduddur.
Böyrək funksiyası pozulmuş pasiyentlər
Böyrək çatışmazlığı olan pasiyentlərdə dozanın tənzimlənməsi tələb olunmur. Böyrək xəstəliyinin son mərhələsində olan pasiyentlərdə Semavic® preparatının istifadə təcrübəsi yoxdur; belə pasiyentlərdə Semavic® preparatının istifadəsi əks-göstərişdir.
Qaraciyər funksiyası pozulmuş pasiyentlər
Qaraciyər çatışmazlığı olan pasiyentlərdə dozanın tənzimlənməsi tələb olunmur (“Farmakokinetika” bölməsinə baxın). Ağır dərəcəli qaraciyər çatışmazlığı olan pasiyentlərdə semaqlutidin istifadə təcrübəsi məhduddur; belə pasiyentlərdə Semavic® preparatının istifadəsi əks-göstərişdir.
Əlavə təsirlər
KT zamanı ən çox qeydə alınan əlavə təsirlər (ƏT) MBT tərəfindən pozulmalar, o cümlədən ürəkbulanma, ishal və qusma olmuşdur. Ümumilikdə, bu təsirlər yüngül və ya orta dərəcəli və qısamüddətli olmuşdur. Semavic® preparatının istifadəsi zamanı yaranması mümkün olan əlavə təsirlər ÜST-nin tövsiyələrinə əsasən baş vermə tezlikləri göstərilməklə, tənzimləyici fəaliyyət üçün MedDRA lüğətinə uyğun olaraq sistem-orqan sinifləri üzrə bölünmüşdür: çox tez-tez: (≥1/10), tez-tez (≥1/100, lakin <1/10), bəzən (≥1/1 000, lakin <1/100), nadir hallarda (≥1/10 000, lakin <1/1 000), çox nadir hallarda (<1/10 000), naməlum tezlikdə (mövcud məlumatlar əsasında qiymətləndirmək mümkün deyil). İnkişaf etmə tezliyi üzrə hər bir qrupda ƏT ciddilik dərəcəsinin azalması ardıcıllığı ilə göstərilmişdir.
Cədvəl 1. 3-cü faza KT-nin keçirilməsi zamanı aşkar edilmiş əlavə təsirlər
| MedDRA orqanlar sistemi | Çox tez-tez | Tez-tez | Bəzən | Nadir hallarda |
|---|---|---|---|---|
| İmmun sistemi tərəfindən pozulmalar | Anafilaktik reaksiyalar | |||
| Maddələr mübadiləsi və qidalanma tərəfindən pozulmalar | Hipoqlikemiya⁽ᵃ⁾ insulin və ya sulfonil sidik cövhəri törəməsi ilə birlikdə istifadə zamanı | Hipoqlikemiya⁽ᵃ⁾ digər PHQP ilə birlikdə istifadə zamanı İştahanın azalması | ||
| Sinir sistemi tərəfindən pozulmalar | Başgicəllənmə | Disgevziya | ||
| Görmə orqanı tərəfindən pozulmalar | Diabetik retinopatiyanın ağırlaşmaları⁽ᵇ⁾ | |||
| Ürək tərəfindən pozulmalar | Ürək yığılmalarının tezliyinin (ÜYT) artması | |||
| MBT tərəfindən pozulmalar | Ürəkbulanma, ishal | Qusma, qarında ağrı, qarında köp, qəbizlik, dispepsiya, qastrit, qastroezofageal reflüks xəstəliyi, gəyirmə, meteorizm | ||
| Qaraciyər və ödçıxarıcı yollar tərəfindən pozulmalar | Xolelitiaz | |||
| Ümumi pozulmalar və yeridilmə yerində dəyişikliklər | Yorulma | Yeridilmə yerində reaksiyalar | ||
| Laborator və instrumental məlumatlar | Lipazanın aktivliyinin artması, amilazanın aktivliyinin artması, bədən çəkisinin azalması |
⁽ᵃ⁾qan plazmasında qlükozanın konsentrasiyasının < 3,1 mmol/l olması ilə birlikdə ağır (digər şəxsin köməyini tələb edən) və ya simptomatik kimi müəyyən edilmiş hipoqlikemiya
⁽ᵇ⁾diabetik retinopatiyanın ağırlaşmaları — aşağıdakıların kombinasiyasıdır: gözün torlu qişasının fotokoaqulyasiyasına ehtiyac, preparatların intravitreal yeridilməsinə ehtiyac, şüşəvarı cismə qansızma, ŞD ilə əlaqəli korluğun inkişaf etməsi
Tezlik ÜD nəticələrinin tədqiqinə əsaslanmışdır.
Ayrı-ayrı əlavə təsirlərin təsviri
Hipoqlikemiya
Semavic® preparatı ilə monoterapiya zamanı ağır hipoqlikemiya epizodları müşahidə edilməmişdir. Ağır dərəcəli hipoqlikemiya, əsasən, Semavic® preparatının sulfonil sidik cövhərinin törəməsi və ya insulinlə kombinasiyada istifadəsi zamanı müşahidə olunmuşdur. Semavic® preparatının sulfonil sidik cövhərinin törəməsi istisna olmaqla, digər PHQP ilə kombinasiyada istifadəsi zamanı bir neçə ağır hipoqlikemiya epizodu müşahidə olunmuşdur.
MBT tərəfindən ƏT
0,5 mq və 1 mq dozada Semavic® preparatı ilə müalicə zamanı pasiyentlərdə ürəkbulanma, ishal və qusma qeydə alınmışdır. Əlavə təsirlərin əksəriyyəti yüngül dərəcədən orta dərəcəyədək və qısamüddətli olmuşdur. ƏT pasiyentlərin müvafiq olaraq 3,9 % və 5,9 %-nin KT-dən vaxtından əvvəl çıxmasına səbəb olmuşdur. ƏT barədə daha çox müalicənin ilk aylarında məlumat verilmişdir.
Diabetik retinopatiyanın ağırlaşmaları
Uzun müddət davam edən ŞD2 və ÜD xəstəliklərinin yüksək riski olan və qlikemik nəzarətin yetərli olmadığı pasiyentlərin iştirakı ilə keçirilmiş 2 illik KT-də ağırlaşmış diabetik retinopatiyanın təsdiqlənmiş halları plasebo qəbul edən pasiyentlərlə (1,8 %) müqayisədə Semavic® preparatı qəbul edən daha çox pasiyentdə (3,0 %) inkişaf etmişdir. KT-nin əvvəlində anamnezində diabetik retinopatiyanın olduğu pasiyentlərdə ağırlaşmaların inkişaf etməsinin mütləq riski daha yüksək olmuşdur. Anamnezində diabetik retinopatiyanın olması təsdiqlənməmiş pasiyentlərdə hadisələrin sayı Semavic® preparatının və plasebonun istifadəsi zamanı eyni olmuşdur. 1 ilədək davam edən KT-də diabetik retinopatiya ilə əlaqəli ƏT-lərin tezliyi Semavic® preparatı qrupunda və müqayisə preparatları qruplarında eyni olmuşdur.
ƏT səbəbindən müalicənin dayandırılması
1 mq Semavic® preparatı qəbul edən pasiyentlər arasında ƏT səbəbindən müalicənin dayandırılması hallarının tezliyi 8,7 % olmuşdur. Müalicənin dayandırılmasına gətirib çıxaran ən çox rast gələn ƏT MBT tərəfindən pozulmalar olmuşdur.
Yeridilmə yerində reaksiyalar
0,5 mq və 1 mq semaqlutid qəbul edən pasiyentlərin müvafiq olaraq 0,6 % və 0,5 %-də yeridilmə yerində reaksiyalar (məsələn, yeridilmə yerində səpgi, qızartı) barədə məlumat verilmişdir. Bu reaksiyalar, bir qayda olaraq, yüngül xarakterli olmuşdur.
İmmunogenlik
Zülal və peptid tərkibli dərman preparatlarının potensial immunogen xüsusiyyətləri səbəbindən Semavic® preparatı ilə müalicədən sonra pasiyentlərdə semaqlutidə qarşı anticisimlər yarana bilər. KT-nin sonunda istənilən vaxt semaqlutidə qarşı anticisimlərin aşkar edildiyi pasiyentlərin payı aşağı (1–2 %) olmuş və heç bir pasiyentdə semaqlutidə qarşı neytrallaşdırıcı anticisimlər və ya endogen QBP-1-i neytrallaşdırıcı təsirə malik olan anticisimlər aşkar edilməmişdir.
İstifadə təlimatında göstərilmiş əlavə təsirlərin hər hansı biri şiddətlənərsə və ya hər hansı digər əlavə təsirlər yaranarsa, bu barədə həkimə məlumat vermək lazımdır.
Doza həddinin aşılması
Simptomlar
KT-nin gedişində birdəfəlik dozada 4 mq-dək və həftədə 4 mq-dək doza həddinin aşılması halları barədə məlumat verilmişdir. Barəsində ən çox məlumat verilmiş ƏT ürəkbulanma olmuşdur. Bütün pasiyentlər ağırlaşma olmadan sağalmışdır.
Müalicə
Semavic® preparatının doza həddinin aşılması zamanı xüsusi antidot mövcud deyildir. Doza həddinin aşılması zamanı müvafiq simptomatik müalicənin aparılması tövsiyə olunur. Preparatın xaricolma müddətinin uzun (təxminən 1 həftə) olmasını nəzərə alaraq, doza həddinin aşılmasının uzun müddət müalicə və müşahidə olunması tələb oluna bilər.
Digər dərman vasitələri ilə qarşılıqlı təsiri
Farmakodinamik qarşılıqlı təsir
Semaqlutidin in vitro şəraitində aparılmış tədqiqatları sitoxrom P450 (CYP) sistemi fermentlərinin inhibə və ya induksiya olunması və dərman preparatlarının daşıyıcılarının inhibə olunması ehtimalının çox az olduğunu göstərmişdir. Semaqlutidin istifadəsi zamanı mədənin boşalmasının ləngiməsi yanaşı qəbul edilən peroral dərman preparatlarının sorulmasına təsir göstərə bilər.
MBT-dən sürətlə sorulması tələb olunan peroral dərman preparatları qəbul edən pasiyentlərdə semaqlutid ehtiyatla istifadə edilməlidir.
Parasetamol
Standartlaşdırılmış qida qəbulu sınağında parasetamolun farmakokinetikasının qiymətləndirilməsi zamanı aşkar edilmişdir ki, semaqlutid mədənin boşalmasını ləngidir. 1 mq semaqlutidin eyni zamanda qəbulu zamanı parasetamolun AUC0–60 dəq və Cmax göstəriciləri müvafiq olaraq 27 % və 23 % azalmışdır. Bu zaman parasetamolun ümümi ekspozisiyası (AUC0–5 saat) dəyişməmişdir. Semaqlutidin və parasetamolun eyni zamanda qəbulu zamanı parasetamolun dozasının tənzimlənməsi tələb olunmur.
Peroral hormonal kontraseptiv vasitələr
Semaqlutidin peroral hormonal kontraseptiv vasitələrin effektivliyini azaltdığı ehtimal edilmir. Kombinə olunmuş peroral hormonal kontraseptiv preparat (0,03 mq etinilestradiol/0,15 mq levonorgestrel) ilə semaqlutidin eyni zamanda istifadəsi zamanı semaqlutid etinilestradiolun və levonorgestrelin ümumi ekspozisiyasına klinik cəhətdən əhəmiyyətli təsir göstərməmişdir. Etinilestradiolun ekspozisiyası dəyişilməz qalmışdır; tarazlıq vəziyyətində levonorgestrelin ekspozisiyasının 20 % artması müşahidə olunmuşdur. Komponentlərin heç biri üçün Cmax dəyişməmişdir.
Atorvastatin
Atorvastatinin birdəfəlik dozasının (40 mq) istifadəsindən sonra semaqlutid atorvastatinin sistem ekspozisiyasını dəyişdirməmişdir. Atorvastatinin Cmax göstəricisi 38 % azalmışdır. Bu dəyişiklik klinik cəhətdən əhəmiyyətsiz hesab edilmişdir.
Diqoksin
Diqoksinin birdəfəlik dozasının (0,5 mq) istifadəsindən sonra semaqlutid diqoksinin sistem ekspozisiyasını və ya Cmax göstəricisini dəyişdirməmişdir.
Metformin
Metforminin 3,5 gün ərzində gündə 2 dəfə 500 mq dozada istifadəsindən sonra semaqlutid metforminin sistem ekspozisiyasını və ya Cmax göstəricisini dəyişdirməmişdir.
Varfarin
Varfarinin birdəfəlik dozasının (25 mq) istifadəsindən sonra semaqlutid varfarinin R- və S-izomerlərinin sistem ekspozisiyasını və ya Cmax göstəricisini dəyişdirməmişdir. Beynəlxalq normallaşdırılmış nisbətin (BNN) tərifinə əsasən, varfarinin farmakodinamik təsirlərinin də klinik cəhətdən əhəmiyyətli dəyişiklikləri müşahidə edilməmişdir.
Uyuşmazlıq
Semavic® preparatını digər dərman vasitələri ilə, o cümlədən infuziya məhlulları ilə qarışdırmaq olmaz. Semavic® preparatına əlavə edilən maddələr semaqlutidin parçalanmasına səbəb ola bilərlər.
Xüsusi göstərişlər
Semavic® preparatının ŞD1 olan pasiyentlərdə və ya diabetik ketoasidozun müalicəsi üçün istifadəsi əks-göstərişdir. Semavic® preparatı insulini əvəz etmir
MBT tərəfindən reaksiyalar
QBP-1R aqonistlərinin istifadəsi MBT tərəfindən ƏT ilə əlaqələndirilə bilər. Böyrək çatışmazlığı olan pasiyentlərin müalicəsi zamanı bunu nəzərə almaq lazımdır, belə ki, ürəkbulanma, qusma və ishal dehidratasiyaya və böyrəklərin funksiyasının pisləşməsinə gətirib çıxara bilər.
Kəskin pankreatit
QBP-1R aqonistlərinin istifadəsi zamanı kəskin pankreatitin inkişaf etməsi halları müşahidə edilmişdir. Pasiyentlər kəskin pankreatitin səciyyəvi simptomları barədə məlumatlandırılmalıdırlar. Pankreatitə şübhə olduqda, Semavic® preparatı ilə müalicə dayandırılmalıdır; kəskin pankreatit təsdiqləndiyi halda Semavic® preparatı ilə müalicə bərpa edilməməlidir. Anamnezində pankreatit olan pasiyentlərdə ehtiyatlı olmaq lazımdır. Kəskin pankreatitin digər əlamət və simptomları mövcud olmadıqda, mədəaltı vəzi fermentlərinin aktivliyinin artması kəskin pankreatitin inkişaf etməsinin proqnostik amili deyildir.
Hipoqlikemiya
Semavic® preparatını sulfonil sidik cövhərinin törəməsi və ya insulinlə kombinasiyada qəbul edən pasiyentlərdə hipoqlikemiyanın inkişaf etmə riski yüksək ola bilər. Semavic® preparatı ilə müalicənin əvvəlində sulfonil sidik cövhəri törəməsinin və ya insulinin dozasını azaltmaqla hipoqlikemiyanın inkişaf etmə riskini azaltmaq olar.
Diabetik retinopatiya
Diabetik retinopatiyası olan, insulin və semaqlutid ilə müalicə qəbul edən pasiyentlərdə diabetik retinopatiyanın ağırlaşmalarının inkişaf etmə riskinin artması müşahidə olunmuşdur (“Əlavə təsirləri” bölməsinə baxın). Diabetik reinopatiyası olan və insulinlə müalicə qəbul edən pasiyentlərdə semaqlutidin istifadəsi zamanı ehtiyatlı olmaq lazımdır. Belə pasiyentlər daimi müşahidə altında olmalı və klinik tövsiyələrə uyğun olaraq müalicə qəbul etməlidirlər. Qlikemik nəzarətin sürətlə yaxşılaşması diabetik retinopatiya vəziyyətinin müvəqqəti pisləşməsi ilə əlaqələndirilmişdir, lakin eyni zamanda digər səbəbləri də istisna etmək olmaz.
Ürək çatışmazlığı
NYHA təsnifatı üzrə IV funksional sinif XÜÇ olan pasiyentlərdə Semavic® preparatının istifadə təcrübəsi mövcud deyil. Belə pasiyentlərdə preparatın istifadəsi əks-göstərişdir.
Qalxanabənzər vəzinin xəstəlikləri
Qeydiyyatdan sonrakı dövrdə digər bir QBP-1 analoqu olan liraqlutidin istifadəsi zamanı qalxanabənzər vəzinin medullyar xərçəngi (QVMX) halları qeydə alınmışdır. QVMX-nin yaranması ilə QBP-1 analoqlarının istifadəsi arasında səbəb-nəticə əlaqəsinin müəyyən olunması və ya istisna edilməsi üçün mövcud məlumatlar kifayət deyil. Pasiyenti QVMX və qalxanabənzər vəzi şişinin simptomları (boyun nahiyəsində bərkləşmənin yaranması, disfagiya, təngnəfəslik, səsin daim xırıltılı olması) barədə məlumatlandırmaq lazımdır. Qan plazmasında kalsitoninin konsentrasiyasının əhəmiyyətli dərəcədə yüksəlməsi QVMX-ni göstərə bilər (QVMX olan pasiyentlərdə qan plazmasında kalsitoninin konsentrasiyasının dəyərləri adətən 50 nq/l-dən böyük olur) Qan plazmasında kalsitoninin konsentrasiyasının yüksəlməsi aşkar edildikdə, pasiyentin sonrakı müayinəsi aparılmalıdır. Tibbi müayinə zamanı və ya qalxanabənzər vəzinin USM müayinəsində qalxanabənzər vəzidə düyünləri aşkar edilmiş pasiyentlər də əlavə olaraq müayinə olunmalıdırlar. Şəxsi və ya ailə anamnezində QVMX və ya tip 2 ÇEN sindromu olan pasiyentlərdə semaqlutidin istifadəsi əks-göstərişdir.
Preklinik təhlükəsizlik məlumatları
Farmakoloji təhlükəsizlik, təkrar dozaların toksikliyi və genotoksiklik üzrə tədqiqatlara əsaslanan preklinik məlumatlar insan üçün hər hansı təhlükəni aşkara çıxarmamışdır. Siçovullar və siçanlar üzərində aparılmış kanserogenlik üzrə 2 illik tədqiqatlarda semaqlutid klinik cəhətdən əhəmiyyətli konsentrasiyalarda qalxanabənzər vəzinin C-hüceyrələrinin ölümlə nəticələnməyən şişlərinin inkişafına səbəb olmuşdur. Siçovullarda qalxanabənzər vəzinin C-hüceyrələrinin ölümlə nəticələnməyən şişləri QBP-1 analoqları qrupu üçün səciyyəvidir. İnsanlarda bu riskin aşağı olduğu hesab edilir, lakin tamamilə istisna edilə bilməz.
Fertillik
İnsanlarda semaqlutidin fertilliyə təsiri məlum deyil. Semaqlutid dişi siçovullarda fertilliyə təsir etməmişdir. Dişi siçovullar arasında estral siklin artması və ovulyasiyaların sayının cüzi azalması dişi siçovulun bədən çəkisinin azalması ilə müşayiət olunan dozalarda müşahidə olunmuşdur.
Nəqliyyat vasitələrini və mexanizmləri idarə etmək qabiliyyətinə təsiri
Semavic® preparatı nəqliyyat vasitələrini idarə etmək və ya mexanizmlərlə işləmək qabiliyyətinə təsir etmir və ya cüzi təsir edir. Pasiyentlər, xüsusilə də, Semavic® preparatının sulfonil sidik cövhəri törəməsi və ya insulinlə birlikdə istifadəsi zamanı nəqliyyat vasitələrini idarə edərkən və mexanizmlərlə işləyərkən onlarda hipoqlikemiyanın inkişaf etməsinə yol verməmək üçün ehtiyat tədbirlərinə riayət etməli olduqları barədə xəbərdar edilməlidirlər.
İstifadə üzrə təlimat
Semavic® preparatının əvvəlcədən doldurulmuş şpris-qələmi 0,25 mq, 0,5 mq və 1 mq dozaları yeritməyə imkan verir. Bir şpris-qələmdə 3 ml məhlul vardır. Semavic® preparatının qablaşmasına birdəfəlik iynələr daxildir. Pasiyentlərə hər bir inyeksiyadan sonra inyeksiya iynəsini yerli tələblərə uyğun olaraq atmaları tövsiyə olunmalıdır. Semavic® şpris-qələmi yalnız fərdi istifadə üçün nəzərdə tutulmuşdur. Şəffaf, rəngsiz və ya demək olar ki, rəngsiz məhlul şəklində görünmədikdə, Semavic® preparatını istifadə etmək olmaz. Dondurulmuş olduğu halda Semavic® preparatını istifadə etmək olmaz. Semavic® preparatı uzunluğu 8 mm-ə qədər olan iynələrin köməyi ilə yeridilə bilər. Şpris-qələm birdəfəlik inyeksiya iynələri ilə istifadə üçün nəzərdə tutulmuşdur. Həmişə hər bir inyeksiyadan sonra iynəni çıxarın və Semavic® şpris-qələmini iynəsi çıxarılmış şəkildə saxlayın. Bu, iynələrin tıxanmasının, çirklənmənin, yoluxmanın, məhlulun axmasının və preparatın düzgün olmayan dozasının yeridilməsinin qarşısını almağa kömək edəcəkdir.
Buraxılış forması
Dərialtı yeridilmə üçün məhlul, 1,34 mq/ml Rezin plunjerlərə malik olan, neytral şüşədən hazırlanmış, alüminiumdan kombinə olunmuş rezin diskli qapaqcıqlarla bağlanmış rəngsiz kartriclərdə 3 ml preparat. Kartric çoxsaylı inyeksiyalar üçün çoxdozalı, birdəfəlik plastik şpris-qələmə quraşdırılır. Hər bir şpris-qələmin korpusuna polipropilen plyonkadan etiket yapışdırılır. Çoxsaylı inyeksiyalar üçün 1 ədəd əvvəlcədən doldurulmuş çoxdozalı birdəfəlik şpris-qələm və 9 ədəd birdəfəlik iynə dərman preparatının tibbi istifadə təlimatı və şpris-qələmin istifadəsi üzrə təlimatla birlikdə karton qutuya yerləşdirilir.
Yararlılıq müddəti
2 il. Şpris-qələmin etiketində və qablaşmanın üzərində göstərilmiş müddət başa çatdıqdan sonra istifadə etməyin.
Saxlanma şərtləri
2 °С-dən 8 °С-dək temperaturda (soyuducuda), lakin dondurucu kameradan uzaqda saxlayın. İşıqdan qoruyun. Dondurmayın. İçərisində preparatın olduğu istifadə edilən və ya ehtiyat qismində bir yerdən başqa yerə daşınan şpris-qələmi 30 °C-dən yuxarı olmayan temperaturda və ya 2 °С-dən 8 °С-dək temperaturda (soyuducuda) 9 həftə ərzində saxlamaq olar. Dondurmayın. İstifadə etdikdən sonra işıqdan qorumaq üçün şpris-qələmi qapağı ilə bağlayın. Semavic® preparatını izafi istiliyin və işığın təsirindən qorumaq lazımdır. Uşaqların əllərinin çatmadığı yerdə saxlayın.
Aptekdən buraxılma şərtləri
Reseptlə buraxılır.
Adına dərman vasitəsinin dövlət qeydiyyatı haqqında vəsiqənin verildiyi hüquqi şəxs
ООО “GEROPHARM”, Rusiya Federasiyası, 191119, Sankt-Peterburq şəh., Zveniqorodskaya küç., ev 9. Telefon: (812) 703-79-75 (çoxkanallı), faks: (812) 703-79-76
İstehsalçı
ООО “GEROPHARM”, Rusiya Federasiyası
İstehsalçı
ООО “GEROPHARM”, Rusiya Federasiyası
İstehsal prosesinin bütün mərhələləri:
1. 142279, Rusiya, Moskva vilayəti, Serpuxov şəhər dairəsi, Obolensk fəhlə qəsəbəsi, “Məhəllə A” ərazisi, tikili 5, korpus 1
2. 142279, Rusiya, Moskva vilayəti, Serpuxov şəhər dairəsi, Obolensk fəhlə qəsəbəsi, “Məhəllə A” ərazisi, tikili 4, korpus 82
İstehlakçılardan iradları qəbul edən təşkilat:
Rusiya Federasiyası, ООО “GEROPHARM”, 196608, Sankt-Peterburq şəh., Puşkin şəh., Yaçevski keçidi, ev 4, tikili 1. Telefon: +7 (812) 493-55-01 Faks: +7 (812) 493-55-69 Qaynar xətt telefonu: 8-800-333-4376 (Rusiya üzrə zəng pulsuzdur) Veb-sayt: www.geropharm.ru
Əlavə təsirlər barədə informasiyanı inform@geropharm.ru; farmakonadzor@geropharm.com elektron poçt ünvanlarına və ya ООО “GEROPHARM” şirkətinin yuxarıda göstərilmiş əlaqə məlumatları vasitəsilə göndərməyinizi xahiş edirik.
UnoPen GM-B1 pen-inyektoru çoxsaylı inyeksiyalar üçün əvvəlcədən doldurulmuş, içərisində qlükaqonabənzər peptid-1 (QBP-1) analoqu olan hipoqlikemik vasitə — Semaqlutid olan birdəfəlik şpris-qələmdən (bundan sonra “Şpris-qələm” adlandırılacaq) ibarətdir. Semavic® (0,25 mq/doza, 0,5 mq/doza, 1,0 mq/doza) — əvvəlcədən doldurulmuş şpris-qələmdə dəri altına yeridilmə üçün məhlul 0,25 mq, 0,5 mq və 1,0 mq dozaları yeritməyə imkan verir. Şpris-qələm 0,25 mq dozanın titrlənməsi və 0,5 mq və 1,0 mq terapevtik dozanın dəstəklənməsi üçün nəzərdə tutulmuşdur. Bir şpris-qələmdə 3 ml məhlul vardır.
Semavic® preparatının yeridilməsi zamanı şpris-qələmin istifadə variantları:
1-ci variant - dozanın titrlənməsi
hər biri 0,25 mq olmaqla 4 inyeksiya
hər biri 0,5 mq olmaqla 4 inyeksiya
1,0 mq olmaqla 1 inyeksiya
2-ci variant - terapevtik dozanın dəstəklənməsi
hər biri 1,0 mq olmaqla 4 inyeksiya
Şpris-qələm BD Micro-Fine™ Plus birdəfəlik inyeksiya iynələri ilə birlikdə istifadə üçün nəzərdə tutulmuşdur. Semavic® preparatının qablaşmasına 4 ədəd WellFine 4 mm 32G və ya Dexfine 4 mm 32G və ya Verifine 4 mm 32G iynəsi daxil edilmişdir
Semavic® preparatı uzunluğu 8 mm-ə qədər olan iynələrin köməyi ilə yeridilə bilər.
Hər bir inyeksiyadan əvvəl yeni iynədən istifadə etmək lazımdır. İnyeksiyadan sonra şpris-qələmi iynəsiz saxlamaq və daşımaq lazımdır! Bu, iynələrin tıxanmasının, çirklənmənin, yoluxmanın, məhlulun axmasının və preparatın düzgün olmayan dozasının yeridilməsinin qarşısını alır. İynələri yerli tələblərə uyğun olaraq, potensial yoluxmuş materiallarla rəftar üzrə norma və qaydalara əməl etməklə utilizə etmək lazımdır. Şpris-qələmin istifadəsi yalnız bir şəxs tərəfindən həyata keçirilməlidir. Şpris-qələm üçüncü şəxsə verilməməlidir.
Əgər şpris-qələmdə olan Semavic® preparatı rəngsiz və şəffaf məhluldan fərqli şəkildə görünürsə, onu istifadə etmək olmaz.
Şpris-qələmləri aşağı (+2 °С-dən aşağı) və yüksək (+30 °С-dən yuxarı) temperaturların təsirinə məruz qoymayın. Şpris-qələmləri dondurucu kameraya yerləşdirməyin. Şpris-qələmləri dondurmaq olmaz!
İstifadə edilmiş şpris-qələmlər utilizə olunmalı və təkrar istifadə edilməməlidir (şpris-qələmi təkrar doldurmaq olmaz).
Şpris-qələmləri havanın yüksək/aşağı temperaturlarında xüsusi termopenalda/çantada (məsələn, GEROPHARM şirkətinin orijinal termopenalında) nəql etmək tövsiyə olunur.
Şpris-qələmi və iynələri hamının, xüsusilə də uşaqların əli çatmayan yerlərdə saxlayın.
Şpris-qələmi özünüz təmir etməyə çalışmayın. Şpris-qələm sındıqda, preparatın tibbi istifadəsi üzrə təlimatda göstərilmiş, istehlakçıların iradlarını qəbul edən təşkilata məlumat verin.
GEROPHARM şirkətinin informasiya yardım xəttinin telefonu: 8 (800) 333-43-76.
Əvvəlcədən doldurulmuş (çoxsaylı inyeksiyalar üçün çoxdozalı birdəfəlik) şpris-qələmdə dərialtı yeridilmə üçün məhlul
Əvvəlcədən doldurulmuş Semavic® şpris-qələmini istifadə etməzdən əvvəl bu təlimatı diqqətlə oxuyun.
Şpris-qələmi yalnız həkimin və ya tibb bacısının rəhbərliyi altında onu istifadə etməyi öyrəndikdən sonra istifadə edin.
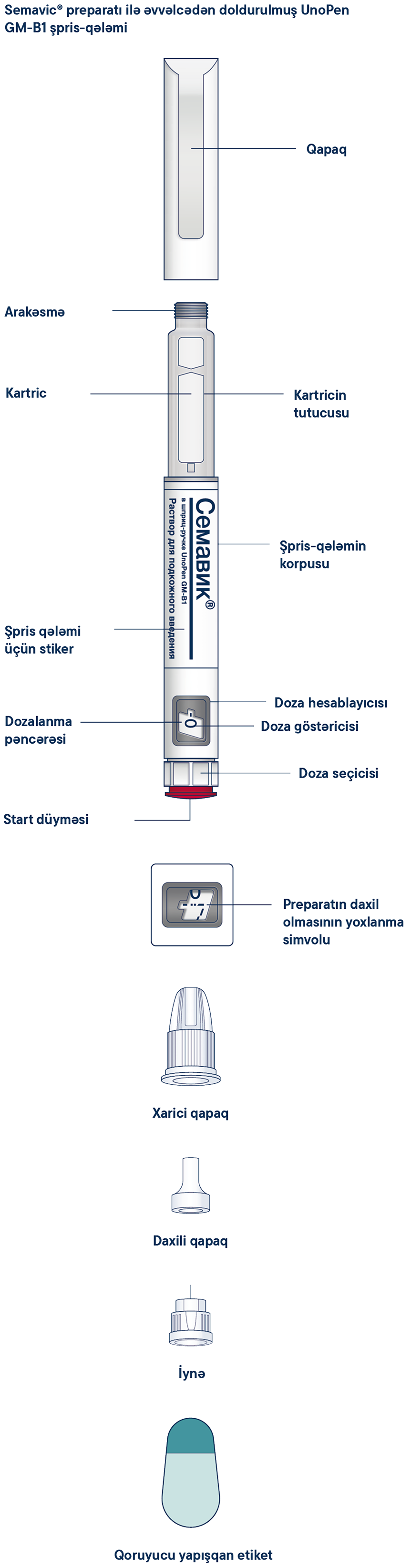
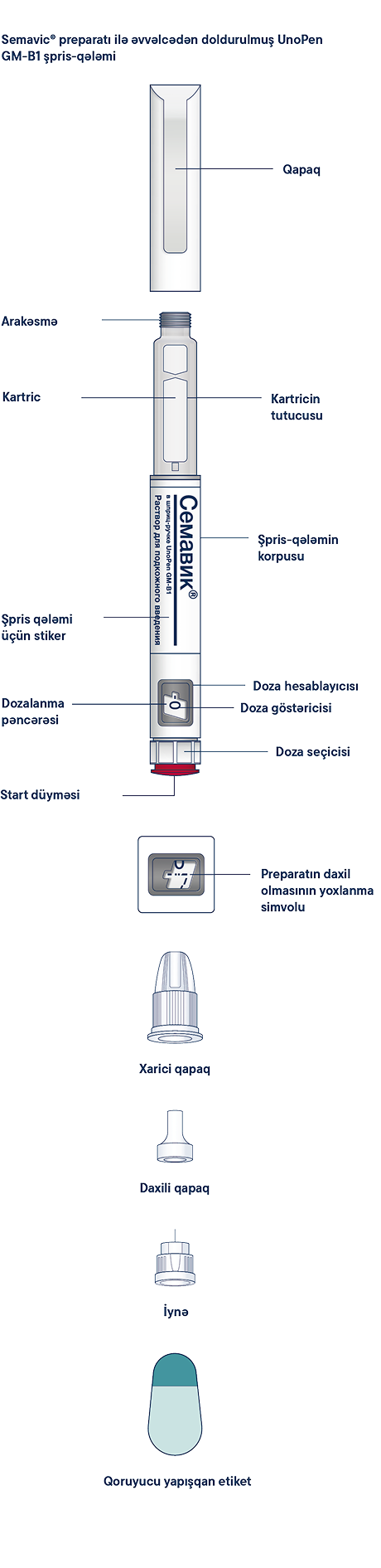
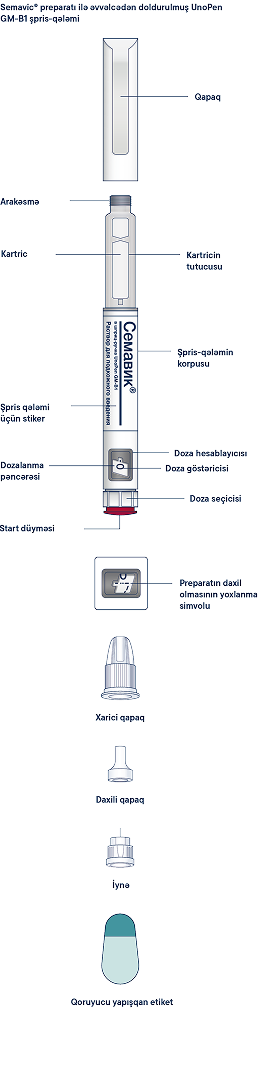
Şpris-qələmin içində Semavic® 0,25 mq/doza, 0,5 mq/doza və ya 1 mq/doza preparatının olduğuna əmin olmaq üçün əvvəlcə şpris-qələmi yoxlayın, daha sonra şpris-qələmin və iynənin müxtəlif hissələri ilə tanış olmaq üçün aşağıda göstərilmiş şəkillərə baxın.
Əgər zəif görürsünüzsə və ya görmə ilə bağlı ciddi problemləriniz varsa və doza hesablayıcısındakı rəqəmləri aydın görə bilmirsinizsə, kənar şəxsin yardımı olmadan şpris-qələmi istifadə etməyin. Sizə görmə qabiliyyəti yaxşı olan, içərisində Semavic® preparatının olduğu əvvəlcədən doldurulmuş şpris-qələmdən istifadə üzrə təlim keçmiş şəxs kömək edə bilər.
Bu şpris-qələm əvvəlcədən doldurulmuş şpris-qələmdir. Onun içərisində 4 mq semaqlutid vardır və 0,25 mq, 0,5 mq və ya 1 mq dozaları seçməyə imkan verir. Şpris-qələm uzunluğu 8 mm-ə qədər olan birdəfəlik iynələrlə istifadə üçün nəzərdə tutulmuşdur.
İynələr qablaşmaya daxildir.
Vacib məlumat
Bu cür işarələrlə qeyd edilmiş informasiyaya xüsusi diqqət yetirin, bu, şpris-qələmin təhlükəsiz istifadəsi üçün çox vacibdir.
Rahat inyeksiyanı təmin etmək və iynələrin tutulmasına yol verməmək üçün həmişə hər bir inyeksiyadan sonra iynəni atın. Əgər iynə tıxanmışdırsa, Siz preparatı özünüzə yeridə bilməyəcəksiniz. İynəsi çıxarılmış boş şpris-qələmi həkim, tibb bacısı, əczaçı tərəfindən verilmiş tövsiyələrə və ya yerli tələblərə uyğun olaraq atın. Heç vaxt daxili qapaqcığı iynəyə yenidən taxmağa cəhd etməyin. İynə ilə özünüzü zədələyə bilərsiniz. Həmişə hər bir inyeksiyadan sonra dərhal iynəni şpris-qələmdən ayırın. Bu, iynələrin tıxanmasının, çirklənmənin, yoluxmanın, məhlulun axmasının və preparatın düzgün olmayan dozasının yeridilməsinin qarşısını almağa kömək edə bilər.
Əlavə vacib məlumatlar
Şpris-qələmə qulluq
Şpris-qələmdən səliqə ilə istifadə edin. Ehtiyatsız rəftar və ya düzgün olmayan istifadə preparatın yanlış dozasının yeridilməsinə gətirib çıxara bilər, nəticədə qanda qlükozanın konsentrasiyası həddən artıq yüksək ola və ya qarın nahiyəsində narahatlıq (ürəkbulanma və ya qusma) baş verə bilər.
Birinci inyeksiyadan əvvəl UnoPen GM-B1 əvvəlcədən doldurulmuş birdəfəlik şpris-qələmlərinin istifadəsi üzrə təlimatı diqqətlə oxumaq və öyrənmək lazımdır.
Şpris-qələmin istifadəsi ilə bağlı müalicə həkimi (mütəxəssis) ilə məsləhətləşmək lazımdır. Şpris-qələmdən düzgün istifadə qaydasını nümayiş etdirməsini xahiş edin. Birinci inyeksiya həkimin və ya tibb bacısının nəzarəti altında aparılmalıdır.
Şpris-qələmin üzərindəki etiketi diqqətlə oxuyun və məhz həkimin Sizə təyin etdiyi preparatı Sizə lazım olan dozada istifadə etdiyinizə əmin olun, eləcə də preparatın yararlılıq müddətini yoxlayın. Daha sonra şpris-qələmin xüsusiyyətləri və tərkib hissələri ilə tanış olmaq üçün aşağıda təqdim edilmiş şəkillərlə tanış olun.
Şpris-qələmdən istifadəyə başlamazdan əvvəl onu mexaniki zədələrin, axıntıların (kartricin hermetikliyinin pozulmasını göstərir) olub-olmaması baxımından yoxlamaq lazımdır. Əgər Siz şpris-qələmin işlək vəziyyətdə olduğuna və zədələnmələrin olmadığına əmin deyilsinizsə, heç vaxt şpris-qələmdən istifadə etməyin. Həmişə hər bir inyeksiyadan əvvəl şpris-qələmi yoxlayın.
Şpris-qələmin istifadə təlimatına ciddi əməl edin: şpris-qələmi əlinizdən yerə salmayın və digər xarici amillərin (termal təsir, düz düşən günəş şüaları, mexaniki zədələnmə və s.) təsirinə yol verməyin. Əgər zədələnmə baş vermişdirsə, yeni şpris-qələmdən istifadəyə başlamaq lazımdır.
Zəif görən pasiyent və ya görmə ilə bağlı ciddi problemləri olan və doza hesablayıcısında olan rəqəmləri aydın görə bilməyən pasiyent şpris-qələmi tibb işçilərinin, qohumlarının və ya görmə qabiliyyəti yaxşı olan, preparatın əvvəlcədən doldurulmuş şpris-qələm vasitəsilə yeridilməsi üzrə təlim keçmiş şəxsin nəzarəti altında istifadə etməlidir.
Xəstələrə qulluq edən şəxslər iynələrin onlara batmasının və çarpaz yoluxmanın qarşısını almaq üçün istifadə edilmiş iynələrlə xüsusi ehtiyatla rəftar etməlidirlər.
Semavic® preparatı ilə əvvəlcədən doldurulmuş UnoPen GM-B1 şpris-qələmi